Acredito que todos os graduando no curso de química, até mesmo alunos do ensino médio já tenham estudado sobre a aromaticidade, fenômeno que, em compostos orgânicos, acontece somente em compostos cíclicos e que tem o benzeno como o exemplo mais comum. Nas minhas aulas dentro deste tópico trabalho um artigo da química nova que trata da evolução histórica deste conceito e apresenta outras duas classificações dos compostos orgânicos: não-aromaticidade e antiaromaticidade.
Caso alguém queira relembrar os conceitos ou por alguma razão nunca ouviu falar, pode acessar o artigo clicando aqui.
Dentre estes compostos ainda existe uma outra classificação. Já ouviu falar em Homoaromaticidade?
O termo Homoaromaticidade é a propriedade de compostos que exibem aromaticidade apesar de uma ou mais ligações saturadas interromperem a conjugação cíclica formal. Entre outras palavras, o fenômeno ocorre em compostos aromáticos onde uma dupla ligação C=C é substituída por um ciclopropano, ou átomo de carbono saturado (SP³) é introduzido na cadeia conjugada.
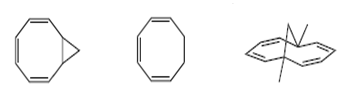 |
| Alguns exemplos de compostos Homoaromáticos |
Uma espécie homoaromática ocorre quando a delocalização cíclica de um sistema com (4n+2) π elétrons não é interrompida pela inserção de um ou mais grupos saturados. Este fenômeno de conjugação não-clássica recebe o nome de homoconjugação e se dá através de três tipos de interações: espacial, por ligações π e transanular. Se considera que o primeiro caso é o mais comum nos sistemas homoaromáticos e recebe o nome de homoconjugação de antiligante; o segundo caso é conhecido como homoconjugação de ligação. No terceiro tipo de interação, diferentemente dos dois anteriores, uma unidade saturada transanular é inserida de tal maneira que causa a perturbação da conjugação direta, mas sem impedi-la.
Teoricamente, derivados dos compostos aromáticos podem ser obtidos, adicionando à estrutura grupos CH2. Como exemplo, temos o íon aromático tropílio e seus derivados. Tal como a conjugação cíclica em aromáticos, a homoconjugação cíclica produz uma diminuição na energia de um sistema homoaromático, fazendo-o mais estável. Porém, estima-se que a estabilização destes sistemas não é tão grande quando comparados com os compostos iniciais aromáticos.