A IUPAC, siga em inglês que significa União Internacional de Química Pura e Aplicada, é o órgão responsável por ditar as regras utilizadas na química. No início de 2011, publicou um artigo apresentando uma definição revisada de Ligação de Hidrogênio. Bom, aquela que nós conhecemos de uma atração eletrostática entre um hidrogênio ligado a um átomo muito eletronegativo fazendo uma interação eletrostática com outro elemento muito eletronegativo não existe mais.
Até o início do século XX uma ligação de hidrogênio era definida exclusivamente como uma interação eletrostática entre um átomo de hidrogênio e um átomo bem mais eletronegativo (átomo com capacidade para atrair pra si elétrons). Além disso, o átomo de hidrogênio envolvido na ligação de hidrogênio teria de ter uma ligação covalente (em que existe um compartilhamento de elétrons) com um átomo de um elemento muito eletronegativo. Em geral o átomo eletronegativo seria um átomo de nitrogênio (N), oxigênio (O) (os elementos envolvidos nas ligações de hidrogênio do DNA) ou flúor (F).
Quando um átomo está ligado covalentemente a um átomo muito eletronegativo é criado um dipolo permanente, em que o átomo de hidrogênio é o “pólo positivo”. Este átomo de hidrogênio tem facilidade para estabelecer uma interação com outro átomo muito eletronegativo. A interação eletrostática criada é facilitada pelo pequeno tamanho do átomo de hidrogênio em relação aos outros átomos.
No entanto, ao longo do século XX foram aparecendo casos de ligações de hidrogênio que não se conformavam à definição oficial da IUPAC. Como as ligações estabelecidas entre moléculas de etileno (C2H4) e moléculas de sulfeto de hidrogênio (H2S). Nem o carbono (presente no etileno) nem o enxofre (presente no sulfeto de hidrogênio) são elementos particularmente eletronegativos, apesar de existir ligações entre estas moléculas envolvendo o átomo de hidrogênio, embora possuindo todas as características de uma ligação de hidrogênio, não podiam receber esse nome.
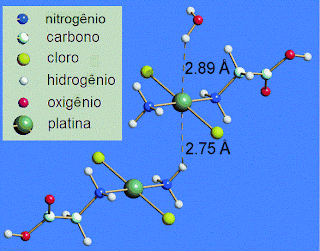
Outro exemplo é o das ligações envolvendo hidrogênio estabelecidas entre moléculas de um complexo, trans-[PtCl2(NH3)N-glycine)]•H2O. Neste caso, como se pode ver pela figura, são estabelecidas ligações intermoleculares entre átomos de platina (Pt) e átomos de hidrogênio (H) que apresentam características de uma ligação de hidrogênio. Mas os átomos de platina são apenas ligeiramente mais eletronegativos que os de hidrogénio. Segundo a nova definição a ligação estabelecida entre os átomos de hidrogênio e os átomos de platina (linha pontilhada) é agora considerada uma ligação de hidrogênio.
Para ter acesso ao artigo na íntegra (em inglês), clique aqui.
Parte do texto foi extraída do blog ema não é uma avestruz.
Parte do texto foi extraída do blog ema não é uma avestruz.

Nenhum comentário:
Postar um comentário